MDREX、米国製造所におけるKGMP現地審査対応および最終KGMP認証の取得
" MDREX、米国製造所におけるKGMP現地審査対応
および最終KGMP認証の取得 "
当社は2025年4月14日から4月20日まで、米国テキサス州への出張に行ってきました。
今回の出張は、米国現地製造所に対するKGMP(韓国GMP)認証審査を支援するためのものであり、
最終的に「適合」判定を受けてKGMP認証を取得し、審査対応を成功裏に完了いたしました。
今回のKGMP審査は、韓国食品医薬品安全処(MFDS)および審査機関(KTR)の厳格な審査基準に基づき、製造所の品質マネジメントシステム(QMS)全般に対して体系的な評価を行う形で実施されました。
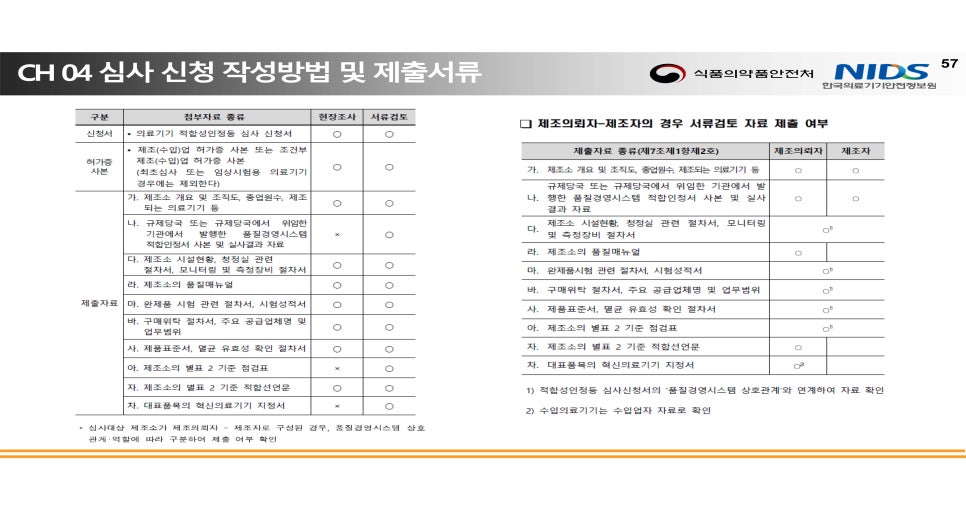
審査の範囲には、品質マニュアル、標準作業手順書(SOP)、設計検証(Verification)および有効性確認(Validation)、製造および工程管理、工程バリデーション(IQ/OQ/PQ)、リスクマネジメント、サプライヤー評価、有害事象報告体制など、KGMPの全要件が含まれました。
MDREX(エムディレックス)は、クライアント製造所と緊密に連携し、以下のようにKGMP審査の準備および現地対応を体系的に支援いたしました。
|
- 審査対応戦略の策定 |
|
- 事前文書のレビューおよび改善 |
|
- 現地審査時の通訳およびリアルタイム対応支援 |
|
- 審査前後の追加補完事項に対する対応策の立案 |
今回の審査をご依頼いただいたクライアントにおかれましては、MDREXの専門的かつ体系的な支援により「適合」判定を受け、最終的にKGMP認証を取得する成果を収めることができました。
特に今回の現地審査では、以下のような改善事項を準備し、現場で効果的に対応することで、
審査官から高い評価を得ることができました。
|
- デバイスマスターレコード(DMR)管理体制の整備 |
|
- KGMP要件を反映した品質文書体系の強化 |
|
- リスクベースのサプライヤー管理プロセスの確立 |
|
- 環境モニタリング体制の構築 |
|
- 韓国医療機器法および関連告示に準拠した安全性情報管理体制の補完 |
今回のKGMP認証を通じて、MDREXは国内だけでなく海外製造所を対象としたKGMP認証およびMFDS承認の取得支援が可能な医療機器専門コンサルティング会社であることを自信を持ってお伝えいたします。
MDREXは今後も、国内外の医療機器製造業者に対する全般的な規制対応業務を支援してまいります。
|
- MFDS製品承認 |
|
- KGMP認証および更新審査対応 |
|
- 品質システムの構築 |
|
- 海外製造所への現地審査支援 |
|
- 品質文書および技術文書の作成支援 |
|
- 市販後安全管理(PSUR、リコール対応等) |
ご不明な点がございましたら、いつでもお気軽にMDREX(エムディレックス)までご連絡ください。
どうぞよろしくお願いいたします。